- Teste de hematologie
- Teste de biochimie
- Biochimie generală din sânge și urina
- Proteine specifice in ser si urina
- Teste biochimice din lichide de punctie
- Teste biochimice din materii fecale
- Teste biochimice pentru tulburari ereditare de metabolism
- Teste pentru nefrolitiaza
- Vitamine, oligoelemente, stres oxidativ
- Acizi grași
- Transferina carbohidrat deficitara (CDT) marker pentru alcoolism
- Markeri non-invazivi pentru afecţiunile hepatice
- Analiza chimică calculi
- Markeri endocrini
- Markeri tumorali
- Markeri virali
- Markeri cardiaci
- Markeri anemie
- Markeri ososi
- Markeri boli autoimune
- Anticorpi antispermatozoizi
- Autoanticorpi in afectiuni endocrine, cardiace, renale
- Autoanticorpi in afectiuni neurologice
- Autoanticorpi in afectiunile dermatologice
- Autoanticorpi in anemia pernicioasa
- Autoanticorpi in diabetul zaharat
- Markeri pentru afectiuni hepatice si gastrointestinale autoimune
- Markeri pentru afectiuni reumatismale si vasculite
- Markeri pentru monitorizarea evolutiei si tratamentului
- Markeri pentru sindromul antifosfolipidic
- Serologie boli infectioase
- Teste specializate de alergologie si imunologie
- Teste de biologie moleculara
- Teste de citogenetica
- Teste de microbiologie
- Toxicologie
- Citologie cervico-vaginala
- Histopatologie
- Consult genetic
- Genetica medicala
Fenobarbital
Preț: 203.00 lei
Informaţii generale şi recomandări pentru testare – Fenobarbital
In practica medicală curentă este recunoscută din ce in ce mai mult importanţa determinării periodice a nivelului in sange al multora din medicamentele administrate, fie datorită potenţialului crescut de reacţii adverse, fie complianţei reduse a pacienţilor.
Monitorizarea terapeutică a unui medicament (Therapeutic Drug Monitoring, TDM) are drept scop menţinerea concentraţiei acestuia in intervalul terapeutic, definit ca acel interval de valori ale nivelului in ser, plasmă sau sange integral in care medicamentul respectiv isi exercită efectele clinice cu reacţii adverse minime pentru majoritatea pacienţilor.
Conceptul de TDM se referă astfel la măsurarea concentraţiei medicamentelor pentru a optimiza si adapta tratamentul la nivel individual (terapie personalizată). Pentru realizarea acestei ţinte terapeutice este important să se cunoască pentru medicamentele administrate date legate de:
–farmacocinetică: studiază efectele medicamentului asupra organismului (relaţia doză-efect);
–farmacodinamică: studiază efectele organismului asupra medicamentelor (absorbţie, distribuţie etc);
–farmacogenetică: studiază modelul genetic al metabolizării medicamentelor luand in considerare variaţiile individuale.
Pentru a obţine rezultate pentru concentraţiile medicamentoase cu utilitate clinică este important ca proba să fie recoltată in asa numita „steady state” (stare de echilibru) in care rata de medicament ce pătrunde in organism este egală cu cea eliminată. Atunci cand o doză fixă de medicament este administrată la intervale de timp regulate, acesta se va acumula in organism in cursul fazei de absorbţie pană este atinsă starea de echilibru; perioada de timp necesară pentru a se ajunge la steady state depinde de timpul de injumătăţire al medicamentului (T1/2), adică timpul in care concentraţia medicamentului in sange se reduce la jumătate. La randul său T1/2 depinde de rata de metabolizare si excreţie. In condiţiile unei distribuţii rapide si uniforme a medicamentului in organism (cinetică de ordinul I), precum si in absenţa unei doze de incărcare, este nevoie de un interval de timp echivalent cu cel puţin 5 T1/2 pentru a obţine steady state (vezi fig. 20.3.1)1;2;4. 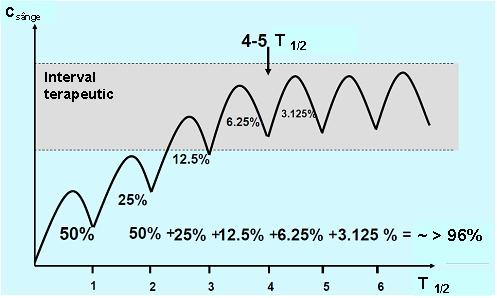
Fig 20.3.1 Obţinerea „steady state”
Acest proces poate fi rezumat astfel:
k k = constanta de dispariţie a lui D
D→E D = concentraţia medicamentului E = forma excretată a medicamentului
k = constanta de dispariţie a lui D
T1/2 = 0.693/k
Asa cum reiese din ecuaţie, T1/2 este o constantă si nu depinde de concentraţia medicamentului. Daca T1/2 este cunoscut se poate calcula modul de impărţire a dozelor si intervalul de timp la care trebuie administrate pentru a se atinge nivelul terapeutic.
Totusi, unele medicamente sunt metabolizate printr-un alt tip de cinetică decat cea de ordinul I, suferind mai intai o metabolizare in ficat, urmată de o distribuţe multicompartimentală in organism (medicamentul are o anumită rată de distribuţie plasmatică si o rată diferită de distribuţie tisulară). In aceste cazuri timpul necesar pentru a atinge steady state poate să fie diferit de echivalentul a 5 T1/2 .
Cu excepţia urgenţelor medicale, in cazurile in care se modifică dozele administrate si se adaugă sau se scot medicamente asociate, se va astepta obţinerea unei noi stări de echilibru inainte de recoltarea probei pentru monitorizarea terapeutică. Intr-un mod similar, se va astepta aceeasi perioadă de timp pană cand un medicament aflat in steady state se va elimina din organism la intreruperea administrării2.
Odată atinsă starea de echilibru probele de sange pot fi recoltate in două momente diferite:
– in momentul nivelului maxim (peak samples): la 2-3 ore după administrarea unei doze orale, la 30-60 minute după o doza administrată intravenos, la 2-4 ore dupa o doză administrată intramuscular sau la 1-1 si ½ ore după o doza administrată intranazal;
– in momentul nivelului minim (trough samples): imediat inaintea administrării următoarei doze; acest moment este recomandat in majoritatea cazurilor.
Monitorizarea terapeutică a medicamentelor este indicată in special in următoarele situaţii:
Clasele de medicamente pentru care se recomandă in mod special TDM sunt următoarele:
- glicozide cardiace: digoxin, digitoxin;
- antiaritmice: amiodarona, flecainida, procainamida, chinidina;
- antiastmatice: teofilina;
- antibiotice: aminoglicozide, vancomicina;
- antivirale: medicamentele pentru infecţia HIV, ganciclovir;
- anticonvulsivante: fenobarbital, carbamazepin, fenitoin, acid valproic, gabapentin, primidona, lamotrigin;
- medicamente psihotrope: litiu, antidepresive triciclice, neuroleptice;
- imunosupresoare: ciclosporina, tacrolimus, sirolimus, everolimus, acid micofenolic, azatioprina;
- citostatice: methotrexat1;2.
In tabelul de mai jos sunt precizate pentru anumite medicamente T1/2, intervalul de timp necesar pentru a se ajunge la steady state, tipul de probă pentru TDM si stabilitatea acesteia, intervalul terapeutic1;4:
|
MEDICAMENT |
T1/2 |
T până la steady state |
Tip probă |
Stabilitate probă |
Metoda de determinare |
Interval terapeutic |
|
Digoxin |
36-48 h |
7-10 zile |
Ser |
7 zile
la 2-8°C
|
ECLIA |
0.9-2 ng/mL |
|
Amiodarona |
26-107 zile |
Nu se aplica | Ser |
7 zile
la 2-8°C
|
HPLC |
0.5-2 mg/L |
|
Flecainida |
12-27 ore |
3-6 zile |
Ser |
7 zile
la 2-8°C
|
HPLC |
0.2-0.8 mg/L |
|
Teofilina |
7-11 ore (adult)
1-8 ore (copil) |
15-55 ore (adult) 5-40 ore (copil) |
Ser |
7 zile
la 2-8°C
|
HPLC |
< 1 an:
5-10 mg/L
≥ 1 an:
8-20 mg/L
|
|
Vancomicina |
3-8
ore
|
1-2 zile |
Ser |
7 zile
la 2-8°C
|
FPIA |
5 – 10 µg/mL
|
|
Carbamazepin |
14-47 ore (adult) 8-19 ore (copil) |
7-12 zile (adult) 2-4 zile (copil) |
Ser |
7 zile
la 2-8°C
|
HPLC |
4-10 mg/L |
|
9-16 ore (adult) 7-13 ore (copil) |
2-4 zile (adult) 2-4 zile (copil) |
Ser |
7 zile
la 2-8°C
|
CEDIA | 50-100 mg/L | |
|
Topiramat |
19-23 ore |
5 zile |
Ser |
7 zile
la 2-8°C
|
HPLC |
1-10 mg/L |
|
Etosuximid |
50-60 ore (adult) 30 ore (copil) |
8-12 zile (adult) 6-10 zile (copil) |
Ser |
7 zile
la 2-8°C
|
HPLC |
40-100 mg/L |
|
81-117 ore (adult) 40-70 ore (copil) |
17-24 zile (adult) 8-15 zile (copil) |
Ser |
7 zile
la 2-8°C
|
HPLC |
10-40 mg/L |
|
|
Fenitoin |
18-22 ore (adult) 7-29 ore (copil) |
4-8 zile (adult) 2-5 zile (copil) |
Ser |
7 zile
la 2-8°C
|
HPLC |
<14 ani:
10-20 mg/L
>14 ani:
6-14 mg/L
|
|
Gabapentin |
5-7 ore (adult) 4-6 ore (copil) |
1-2 zile (adult) 1-2 zile (copil) |
Ser |
7 zile
la 2-8°C
|
HPLC | 2 – 10 µg/mL |
| Lamotrigin |
15-30 ore (adult) 30 ore (copil) |
3-10 zile (adult) 3-10 zile (copil) |
Ser |
7 zile
la 2-8°C
|
HPLC |
<14 ani:
5-15 mg/L
>14 ani:
1-5 mg/L
|
|
Primidona |
3-7 ore (adult) 4-6 ore (copil) |
16-60 ore (adult) 20-30 ore (copil) |
Ser |
7 zile
la 2-8°C
|
HPLC |
5-15 mg/L |
|
Amitriptilina |
8-51 ore |
2-6 zile | Ser |
7 zile
la 2-8°C
|
LC-MS/MS | 50-300 µg/L |
|
Litiu |
14-30 ore |
2-7 zile |
Ser |
8 ore la temperatura camerei 24 ore la 2-8°C 6 luni la -18°C |
ISE |
Mania acută: 0.6-1.2 mmol/L • Protecţie impotriva viitoarelor episoade la pacienţii cu afecţiune bipolară:
0.8-1.0 mmol/L
• Depresie: 0.5-1.5 mmol/L |
|
Clomipramin |
12-36 ore |
3 saptamani | Ser |
7 zile la 2-8°C |
LC-MS/MS |
90-250 µg/L |
|
Clozapina |
4-66 ore | Nu se aplica |
Ser |
7 zile la 2-8°C |
LC-MS/MS |
350-600 µg/L |
|
Olanzapin |
21-54 ore (adult ≤65 ani); 32-81 ore (adult >65 ani) |
7 zile |
Ser |
7 zile
la 2-8°C |
LC-MS/MS | 10-80 µg/L |
|
Doxepin |
8-25 ore |
2.5-5 zile |
Ser |
7 zile la 2-8°C |
LC-MS/MS |
20-150 µg/L |
|
Imipramin |
6-20 ore |
2-5 zile |
Ser |
7 zile la 2-8°C |
LC-MS/MS | 45-150 µg/L |
|
Maprotilin |
36-105 ore |
14 zile |
Ser |
7 zile la 2-8°C | LC-MS/MS | 125-200 µg/L |
|
Trimipramin |
16-39 ore |
Nu se aplica |
Ser |
7 zile la 2-8°C |
LC-MS/MS |
150-350 µg/L |
|
Haloperidol |
41-41 ore (lactat); 14-28 zile (decanoat) |
3-9 zile (lactat); nu se aplica |
Ser |
7 zile la 2-8°C | LC-MS/MS | 5-16 µg/L |
|
Risperidon |
3 ore (fast metabolizer risperidon); 21 ore (fast metabolizer9-hidroxi-risperidon); 20 ore (slow metabolizer risperidon); 30 ore (slow metabolizer 9-hidroxi-risperidon); |
1 zi (fast metabolizer risperidon); 5-6 zile (fast metabolizer9-hidroxi-risperidon); 5 zile (slow metabolizer risperidon); nu se aplica (slow metabolizer 9-hidroxi-risperidon). |
Ser |
7 zile la 2-8°C |
LC-MS/MS |
10-120 µg/L |
|
Ciclosporina A |
6-27 ore |
2-6 zile |
Sânge EDTA |
5 zile la -20°C |
LC-MS/MS |
Intervalul terapeutic variază în funcţie de tipul transplantului si perioada de timp de la transplant. Pentru afecţiuni dermatologice şi reumatologice:<100 µg/L Pentru sindrom nefrotic:
60-160 µg/L
|
|
Tacrolimus |
4-35 ore (adult) 4-12 ore (copil) |
2-6 zile (adult)
Nu se aplică la copil |
Sânge EDTA |
5 zile la -20°C |
LC-MS/MS |
– în primele 2 luni de la transplant:
15-20 µg/L
– după 2 luni de la transplant:
8-15 µg/L
|
| Sirolimus |
46-78 ore |
5-7 zile |
Sânge EDTA |
5 zile
la -20°C
|
LC-MS/MS |
4-20 µg/L |
|
Acid micofenolic |
8-18 ore (adult) variabil la copil |
Nu se aplică |
Ser |
7 zile
la 2-8°C
|
HPLC |
1-3.5 µg/mL |
|
Methotrexat |
Cinetică bifazică |
– |
Ser
|
7 zile
la 2-8°C protejat de lumină
|
FPIA | Se asociază cu un risc crescut de toxicitate:
– valorile > 5-10 µmol/L la 24 h de la admistrare – valorile > 0.5-1 µmol/L la 48 h de la administrare – valorile > 0.2 µmol/L la 72 h de la administrare |
ECLIA = metoda imunochimică cu detecţie prin chemiluminiscenţă
HPLC = cromatografie de lichide sub inaltă presiune
LC-MS/MS = cromatografie de lichide cuplată cu spectrometrie de masă
FPIA = fluorescent polarization immunoassay (metoda imunochimică cu detecţie prin fluorescenţă polarizată)
CEDIA = cloned enzyme donor immunoassay (metoda imunoenzimatică care utilizează tehnologia ADN-ului recombinant)
ISE = ion selective electrode (metoda potentiometrică)
Anticonvulsivante
Sunt medicamente utile in tratamentul epilepsiei, in special pentru crizele grand mal, petit mal, psihomotorii, precum si in unele afecţiuni cum ar fi tic douloureux (nevralgia de trigemen). Desi mecanismul de acţiune al acestor medicamente nu a fost elucidat, se pare că toate, posibil cu excepţia fenobarbitalului, blochează influxul de sodiu in neuronii a căror membrană este afectată. In plus, unele medicamente si in special fenitoinul blochează de asemenea influxul secundar de calciu in aceste celule. Fenobarbitalul si, posibil, fenitoinul stabilizează membrana neuronilor afectaţi.
Multe din anticonvulsivante exercită efect asupra convulsiilor grand mal, insă sunt ineficace asupra celor de tip petit mal. Doar etosuximidul si acidul valproic au un efect terpeutic in aceste condiţii.
In concluzie, desi mecanismul de acţiune al anticonvulsivantelor pare să fie similar, acestea diferă in ceea ce priveste specificitatea2.
Fenobarbital
Este un medicament cu acţiune deprimantă asupra sistemului nervos central care s-a dovedit a fi eficace in controlul convulsiilor generalizate si parţiale. Se administrează frecvent in asociere cu fenitoinul sau cu acidul valproic.
Dozele zilnice de fenobarbital variază intre 60 mg si 300 mg la adult si intre 3 si 6 mg/kg corp la copil. Absorbţia sa este lenta, dar completa cu o biodisponibilitate ce se apropie de 100%. Se leagă intr-un procent de ~50% de proteinele plasmatice si are un volum de distribuţie de 0.5 L/kg; timpul mediu de injumătăţire este de 96 ore, fără metaboliţi activi cunoscuţi. Sedarea apare frecvent la concentraţii terapeutice ale fenobarbitalului in primele 2-3 săptămani de tratament, dar acest efect dispare in timp.
Toxicitatea indusă de supradozare se caracterizează prin depresie SNC, inclusiv a centrilor respiratori. La concentraţii serice >40 mg/L apar simptome usoare precum ataxie, nistagmus, astenie, pierderea atenţiei; simptomele devin severe la nivele >60 mg/L; toxicitatea poate fi letală la valori >100 mg/L.
Nu este cunoscută nici o interacţiune medicamentoasă care să afecteze semnificativ farmacocinetică fenobarbitalul; in schimb acesta perturbă farmacocinetica altor medicamente datorită inducerii sintezei enzimelor asociate citocromului hepatic P4503.
Bibliografie
Produsul a fost adăugat în coș
În plus, ai la dispoziție 30 de zile pentru a veni la recoltare.
