- Teste de hematologie
- Teste de biochimie
- Biochimie generală din sânge și urina
- Proteine specifice in ser si urina
- Teste biochimice din lichide de punctie
- Teste biochimice din materii fecale
- Teste biochimice pentru tulburari ereditare de metabolism
- Teste pentru nefrolitiaza
- Vitamine, oligoelemente, stres oxidativ
- Acizi grași
- Transferina carbohidrat deficitara (CDT) marker pentru alcoolism
- Markeri non-invazivi pentru afecţiunile hepatice
- Analiza chimică calculi
- Markeri endocrini
- Markeri tumorali
- Markeri virali
- Markeri cardiaci
- Markeri anemie
- Markeri ososi
- Markeri boli autoimune
- Anticorpi antispermatozoizi
- Autoanticorpi in afectiuni endocrine, cardiace, renale
- Autoanticorpi in afectiuni neurologice
- Autoanticorpi in afectiunile dermatologice
- Autoanticorpi in anemia pernicioasa
- Autoanticorpi in diabetul zaharat
- Markeri pentru afectiuni hepatice si gastrointestinale autoimune
- Markeri pentru afectiuni reumatismale si vasculite
- Markeri pentru monitorizarea evolutiei si tratamentului
- Markeri pentru sindromul antifosfolipidic
- Serologie boli infectioase
- Teste specializate de alergologie si imunologie
- Teste de biologie moleculara
- Teste de citogenetica
- Teste de microbiologie
- Toxicologie
- Citologie cervico-vaginala
- Histopatologie
- Consult genetic
- Genetica medicala
Litiu
Denumire alternativă: Li
Preț: 37.00 lei
Informatii generale si recomandari pentru testare – Litiu
In practica medicala curenta este recunoscuta din ce in ce mai mult importanta determinarii periodice a nivelului in sange al multora din medicamentele administrate, fie datorita potentialului crescut de reactii adverse, fie compliantei reduse a pacientilor.
Monitorizarea terapeutica a unui medicament (Therapeutic Drug Monitoring, TDM) are drept scop mentinerea concentratiei acestuia in intervalul terapeutic, definit ca acel interval de valori ale nivelului in ser, plasma sau sange integral in care medicamentul respectiv isi exercita efectele clinice cu reactii adverse minime pentru majoritatea pacientilor.
Conceptul de TDM se refera astfel la masurarea concentratiei medicamentelor pentru a optimiza si adapta tratamentul la nivel individual (terapie personalizata). Pentru realizarea acestei tinte terapeutice este important sa se cunoasca pentru medicamentele administrate date legate de:
–farmacocinetica: studiaza efectele medicamentului asupra organismului (relatia doza-efect);
–farmacodinamica: studiaza efectele organismului asupra medicamentelor (absorbtie, distributie etc);
–farmacogenetica: studiaza modelul genetic al metabolizarii medicamentelor luand in considerare variatiile individuale.
Pentru a obtine rezultate pentru concentratiile medicamentoase cu utilitate clinica este important ca proba sa fie recoltata in asa numita „steady state” (stare de echilibru) in care rata de medicament ce patrunde in organism este egala cu cea eliminata. Atunci cand o doza fixa de medicament este administrata la intervale de timp regulate, acesta se va acumula in organism in cursul fazei de absorbtie pana este atinsa starea de echilibru; perioada de timp necesara pentru a se ajunge la steady state depinde de timpul de injumatatire al medicamentului (T1/2), adica timpul in care concentratia medicamentului in sange se reduce la jumatate.
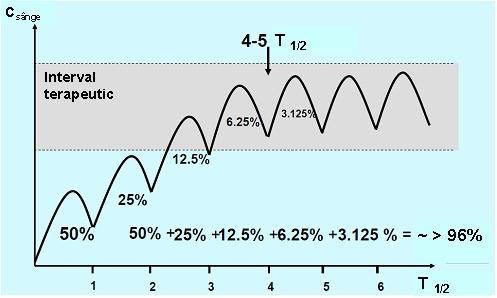
La randul sau T1/2 depinde de rata de metabolizare si excretie. In conditiile unei distributii rapide si uniforme a medicamentului in organism (cinetica de ordinul I), precum si in absenta unei doze de incarcare, este nevoie de un interval de timp echivalent cu cel putin 5 T1/2 pentru a obtine steady state (vezi fig. 20.3.1)3;4;6.
Fig 20.3.1 Obtinerea „steady state”
Acest proces poate fi rezumat astfel:
k
D→E D = concentratia medicamentului E = forma excretata a medicamentului
k = constanta de disparitie a lui D
T1/2 = 0.693/k
Asa cum reiese din ecuatie, T1/2 este o constanta si nu depinde de concentratia medicamentului. Daca T1/2 este cunoscut se poate calcula modul de impartire a dozelor si intervalul de timp la care trebuie administrate pentru a se atinge nivelul terapeutic.
Totusi, unele medicamente sunt metabolizate printr-un alt tip de cinetica decat cea de ordinul I, suferind mai intai o metabolizare in ficat, urmata de o distributie multicompartimentala in organism (medicamentul are o anumita rata de distributie plasmatica si o rata diferita de distributie tisulara). In aceste cazuri timpul necesar pentru a atinge steady state poate sa fie diferit de echivalentul a 5 T1/2 .
Cu exceptia urgentelor medicale, in cazurile in care se modifica dozele administrate si se adauga sau se scot medicamente asociate, se va astepta obtinerea unei noi stari de echilibru inainte de recoltarea probei pentru monitorizarea terapeutica. Intr-un mod similar, se va astepta aceeasi perioada de timp pana cand un medicament aflat in steady state se va elimina din organism la intreruperea administrarii4.
Odata atinsa starea de echilibru probele de sange pot fi recoltate in doua momente diferite:
-in momentul nivelului maxim (peak samples): la 2-3 ore dupa administrarea unei doze orale, la 30-60 minute dupa o doza administrata intravenos, la 2-4 ore dupa o doza administrata intramuscular sau la 1-1 si ½ ore dupa o doza administrata intranazal;
-in momentul nivelului minim (trough samples): imediat inaintea administrarii urmatoarei doze; acest moment este recomandat in majoritatea cazurilor.
Monitorizarea terapeutica a medicamentelor este indicata in special in urmatoarele situatii:
- perturbarea relatiei doza-efect;
- esec in obtinerea efectului terapeutic sau suspectarea unei intoxicatii;
- efect imposibil sau foarte greu de confirmat clinic (de exemplu in cazul imunosupresoarelor);
- interval terapeutic ingust (de exemplu in cazul glicozidelor);
- complianta redusa a pacientilor (persoane varstnice sau cu boli psihice);
- prezenta unor afectiuni care afecteaza absorbtia, distributia, metabolizarea si excretia medicamentelor;
- administrarea simultana de medicamente care prezinta aceeasi cale de eliminare;
- copii si persoane varstnice la care este afectat volumul de distributie: redus in cazul varstnicilor si crescut la copii.
Clasele de medicamente pentru care se recomanda in mod special TDM sunt urmatoarele:
- glicozide cardiace: digoxin. digitoxin;
- antiaritmice: amiodarona, flecainida, procainamida, chinidina;
- antiastmatice: teofilina;
- antibiotice: aminoglicozide, vancomicina;
- antivirale: medicamentele pentru infectia HIV, ganciclovir;
- anticonvulsivante: fenobarbital, carbamazepin, fenitoin, acid valproic, gabapentin, primidona, lamotrigin;
- medicamente psihotrope: litiu, antidepresive triciclice, neuroleptice;
- imunosupresoare: ciclosporina, tacrolimus, sirolimus, everolimus, acid micofenolic, azatioprina;
- citostatice: methotrexat3;4.
In tabelul de mai jos sunt precizate pentru anumite medicamente T1/2, intervalul de timp necesar pentru a se ajunge la steady state, tipul de proba pentru TDM si stabilitatea acesteia, intervalul terapeutic3;6:
| MEDICAMENT | T1/2 | T pana la steady state | Tip proba | Stabilitate proba | Metoda de determinare | Interval terapeutic |
| Digoxin | 36-48 h | 7-10 zile | Ser | 7 zile la 2-8°C | ECLIA | 0.9-2 ng/mL |
| Amiodarona | 26-107 zile | Nu se aplica | Ser | 7 zile la 2-8°C | HPLC | 0.5-2 mg/L |
| Flecainida | 12-27 ore | 3-6 zile | Ser | 7 zile la 2-8°C | HPLC | 0.2-0.8 mg/L |
| Teofilina | 7-11 ore (adult);1-8 ore (copil) | 15-55 ore (adult);5-40 ore (copil) | Ser | 7 zile la 2-8°C | HPLC | < 1 an:5-10 mg/L ≥ 1 an:
8-20 mg/L |
| Vancomicina | 3-8 ore | 1-2 zile | Ser | 7 zile la 2-8°C | FPIA | 5 – 10 µg/mL |
| Carbamazepin | 14-47 ore (adult);8-19 ore (copil) | 7-12 zile (adult);2-4 zile (copil) | Ser | 7 zile la 2-8°C | HPLC | 4-10 mg/L |
| Acid valproic | 9-16 ore (adult);7-13 ore (copil) | 2-4 zile (adult);2-4 zile (copil) | Ser | 7 zile la 2-8°C | CEDIA | 50-100 mg/L |
| Topiramat | 19-23 ore | 5 zile | Ser | 7 zile la 2-8°C | HPLC | 1-10 mg/L |
| Etosuximid | 50-60 ore (adult);30 ore (copil) | 8-12 zile (adult);6-10 zile (copil) | Ser | 7 zile la 2-8°C | HPLC | 40-100 mg/L |
| Fenobarbital | 81-117 ore (adult);40-70 ore (copil) | 17-24 zile (adult);8-15 zile (copil) | Ser | 7 zile la 2-8°C | HPLC | 10-40 mg/L |
| Fenitoin | 18-22 ore (adult);7-29 ore (copil) | 4-8 zile (adult);2-5 zile (copil) | Ser | 7 zile la 2-8°C | HPLC | <14 ani:10-20 mg/L>14 ani:
6-14 mg/L |
| Gabapentin | 5-7 ore (adult);4-6 ore (copil) | 1-2 zile (adult);1-2 zile (copil) | Ser | 7 zile la 2-8°C | HPLC | 2 – 10 µg/mL |
| Lamotrigin | 15-30 ore (adult);30 ore (copil) | 3-10 zile (adult);3-10 zile (copil) | Ser | 7 zile la 2-8°C | HPLC | <14 ani:5-15 mg/L>14 ani:
1-5 mg/L |
| Primidona | 3-7 ore (adult);4-6 ore (copil) | 16-60 ore (adult);20-30 ore (copil) | Ser | 7 zile la 2-8°C | HPLC | 5-15 mg/L |
| Amitriptilina | 8-51 ore | 2-6 zile | Ser | 7 zile la 2-8°C | LC-MS/MS | 50-300 µg/L |
| Litiu | 14-30 ore | 2-7 zile | Ser | 8 ore la temperatura camerei; 7 zile la 2-8°C; 6 luni la -18°C. | ISE | Mania acuta: 0.6-1.2 mmol/L.• Protectie impotriva viitoarelor episoade la pacientii cu afectiune bipolara: 0.8-1.0 mmol/L.• Depresie: 0.5- 1.5 mmol/L |
| Clomipramin | 12-36 ore | 3 saptamani | Ser | 7 zile la 2-8°C | LC-MS/MS | 90-250 µg/L |
| Clozapina | 4-66 ore | Nu se aplica | Ser | 7 zile la 2-8°C | LC-MS/MS | 350-600 µg/L |
| Olanzapin | 21-54 ore (adult≤65 ani);32-81 ore (adult >65 ani) | 7 zile | Ser | 7 zile la 2-8°C | LC-MS/MS | 10-80 µg/L |
| Doxepin | 8-25 ore | 2.5-5 zile | Ser | 7 zile la 2-8°C | LC-MS/MS | 20-150 µg/L |
| Imipramin | 6-20 ore | 2-5 zile | Ser | 7 zile la 2-8°C | LC-MS/MS | 45-150 µg/L |
| Maprotilin | 36-105 ore | 14 zile | Ser | 7 zile la 2-8°C | LC-MS/MS | 125-200 µg/L |
| Trimipramin | 16-39 ore | Nu se aplica | Ser | 7 zile la 2-8°C | LC-MS/MS | 150-350 µg/L |
| Haloperidol | 41-41 ore (lactat);14-28 zile (decanoat) | 3-9 zile (lactat); nu se aplica | Ser | 7 zile la 2-8°C | LC-MS/MS | 5-16 µg/L |
| Risperidon | 3 ore (fast metabolizerrisperidon); 21 ore (fast metabolizer9-hidroxi-risperidon); 20 ore (slow metabolizerrisperidon); 30 ore (slow metabolizer9-hidroxi-risperidon); | 1 zi (fast metabolizerrisperidon); 5-6 zile (fast metabolizer9-hidroxi-risperidon); 5 zile (slow metabolizerrisperidon); nu se aplica (slow metabolizer9-hidroxi-risperidon). | Ser | 7 zile la 2-8°C | LC-MS/MS | 10-120 µg/L |
| Ciclosporina A | 6-27 ore | 2-6 zile | Sange EDTA | 5 zile la -20°C | LC-MS/MS | Intervalul terapeutic variaza in functie de tipul transplantului si perioada de timp de la transplant.Pentru afectiuni dermatologice si reumatologice:<100 µg/LPentru sindrom nefrotic: 60-160 µg/L. |
| Tacrolimus | 4-35 ore (adult);4-12 ore (copil) | 2-6 zile (adult); nu se aplica la copil | Sange EDTA | 5 zile la -20°C | LC-MS/MS | – in primele 2 luni de la transplant:15-20 µg/L- dupa 2 luni de la transplant:
8-15 µg/L |
| Sirolimus | 46-78 ore | 5-7 zile | Sange EDTA | 5 zile la -20°C | LC-MS/MS | 4-20 µg/L |
| Acid micofenolic | 8-18 ore (adult); variabil la copil | Nu se aplica | Ser | 7 zilela 2-8°C | HPLC | 1-3.5 µg/mL |
| Methotrexat | Cinetica bifazica | – | Ser | 7 zilela 2-8°C protejat de lumina | FPIA | Se asociaza cu un risc crescut de toxicitate:- valorile > 5-10 µmol/L la 24 h de la admistrare;- valorile > 0.5-1 µmol/L la 48 h de la administrare;
– valorile > 0.2 µmol/L la 72 h de la administrare. |
ECLIA = metoda imunochimica cu detectie prin chemiluminiscenta
HPLC = cromatografie de lichide sub inalta presiune
LC-MS/MS = cromatografie de lichide cuplata cu spectrometrie de masa
FPIA = fluorescent polarization immunoassay (metoda imunochimica cu detectie prin fluorescenta polarizata)
CEDIA = cloned enzyme donor immunoassay (metoda imunoenzimatica care utilizeaza tehnologia ADN-ului recombinant)
ISE = ion selective electrode (metoda potentiometrica)
Medicamente utilizate in tratamentul tulburarilor maniacale si depresive
Litiul este un metal alcalin monovalent care in mod uzual lipseste din organismul uman. Este folosit in tratamentul psihozelor maniaco-depresive, sub forma de carbonat de litiu. Litiul este complet absorbit dupa administrarea orala in 6-8 ore. Mai putin de 10% din litiu se leaga de proteinele din plasma si timpul de injumatatire este de 14-30 ore. Eliminarea din organism se face in special prin urina, in procent de 95%.
In tratamentul indelungat cu litiu se monitorizeaza osmolaritatea urinara, electrocardiograma, T4, TSH, ureea serica, creatinina si sodiul seric.
Valorile >2 mmol/L indica toxicitate, astfel:
– tremor: 1.5-2.0 mmol/L;
• confuzie/somnolenta: 2.0-2.5 mmol/L;
• convulsii/deces: >2.5 mmol/L.
In general exista o corelatie buna intre concentratia serica a nivelului de litiu si efectul terapeutic/toxic. Totusi unii pacienti fara raspuns terapeutic prezinta niveluri serice adecvate de litiu, dar concentratii eritrocitare reduse. Deoarece litiul actioneaza intracelular, la acesti pacienti determinarea concentratiei eritrocitare de litiu ar putea fi mai relevanta decat cea serica1.
Dieta cu un continut scazut de sodiu determina cresterea concentratiei de litiu prin scaderea excretiei; consumul excesiv de cafeina si sodiu reduc nivelul plasmatic de litiu2.
• Medicamente
Cresteri: diuretice natriuretice (reduc clearance-ul renal al litiului), metronidazol, antiinflamatoare nesteroidiene (ibuprofen), fluoxetin.
Scaderi: metilparaben – substanta prezervanta pentru ser fiziologic steril, N-acetilcisteina5.
• Interferente analitice
In prezenta unui ser hemolizat se pot obtine valori fals crescute.
Electrodul de litiu este usor influentat de prezenta calciului ionic in proba; este posibil sa se obtina valori mai scazute. La valori fiziologic normale ale concentratiei de calciu ionic, influenta acestuia este clinic nesemnificativa.
Se poate determina litiul pentru probe care au sodiul in intervalul 105-180 mmol/L – raspunsul electrodului de litiu depinde de concentratia de sodiu in proba3.
Bibliografie
1. Frances Fischbach. Chemistry Studies. In A Manual of Laboratory and Diagnostic Tests. Lippincott Williams & Wilkins, USA, 7 Ed., 2004, 417.
2. Frances Fischbach. Minerals in Human Nutrition. In A Manual of Laboratory and Diagnostic Tests. Lippincott Williams & Wilkins, USA, 7 Ed., 2004, 1155.
3. Laborator Synevo. Referinte specifice tehnologiei de lucru utilizate. 2010. Ref Type: Catalog.
4. Matthew R. Pincus, Naif Z. Abraham. Toxicology and Therapeutic Drug Monitoring. In Henry’s Clinical Diagnosis and Management by Laboratory Methods, Saunders-Elsevier, 21st Edition, 2007, 308-320.
5. Norbert W Tietz. General Clinical Tests. In Clinical Guide to Laboratory Tests. W.B.SAUNDERS , USA, 3 Ed., 1995; 567.
6. Quest Diagnostics. Therapeutic Drug Monitoring. Drug Half-Life, Steady State, and Recommended Sample Collection Time. www.questdiagnostics.com. Ref Type: Internet Communication.
Produsul a fost adăugat în coș
În plus, ai la dispoziție 30 de zile pentru a veni la recoltare.